Anatomia Vegetal
A anatomia vegetal constitui um ramo da Botânica, onde aspectos das estruturas vegetais são estudados e servem de subsídio para a compreensão da vida das plantas. A anatomia vegetal trata de temas relacionados a morfologia externa e interna das plantas. De acordo com o ambiente onde as espécies se desenvolvem, elas podem apresentar estruturas anatômicas específicas (Appezzato-da-Glória e Carmello-Guerreiro, 2003) que permitem a ocupação dos mais diversos tipos de habitats.
Passe o mouse por sobre o nome das espécies e tecidos e veja as características de cada um.
Blutaparon portulacoides (St - hil) Mears
|
Nome popular: capotiragua, pirixi |
|
|
Nome popular: Cebola |
|
Espaço reservado para outras espécies.
Bibliografia
Appezzato-da-Glória, B e Carmello-Guerreiro, S.M. Anatomia Vegetal. Viçosa: Editora da Universidade Federal de Viçosa, UFV. 2003. 438p.
Boiteux, L. S e Melo, P. C. T. de. 2004. Sistema de Produção de Cebola (Allium cepa L). Embrapa. disponível em: (http://www.cnph.embrapa.br/sistprod/cebola/index.htm). Capturado em março de 2012.
Cordazzo, C.V., Paiva, J.B. & Seeliger, U. Plantas das Dunas da Costa Sudoeste Atlântica. Guia Ilustrado. Pelotas. Ed. USEB. 2006. 107p.
Cordazzo, C.V., e Seeliger, U. Guia Ilustrado Vegetação Costeira no Extremo Sul do Brasil. Rio Grande: Furg. 1995. 275p.
Ferri, M. G. Botânica: Morfologia Interna das Plantas (Anatomia). São Paulo: Edições Melhoramentos, 1970.
Hurrel, J. A.; Uibarri, E. A.; Delucchi, G. e Pochettino, M. L. Biota Rioplatense XIII: Plantas aromáticas condimenticias. Buenos Aires: Lola, 2008, 268p.
Kerbauy, G.B. Fisiologia Vegetal. Rio de Janeiro: Guanabara Koogan, 2004, 452p.
Lorenzi e Matos. Plantas Medicinais no Brasil: Nativas e Exóticas. Nova Odessa: Plantarum, 2002, 512 p.
Raven P. H.; EVERT R. F.; Eichhorn S. E. Biologia Vegetal. 7th ed. Editora Guanabara Koogan S. A., Rio de Janeiro, 2007.Cordazzo e Seeliger, 1995
Smith, W.K.; Volgelmann, T.C.; Delucia, E.H.; Bell,D. T.; Shepherd, K.A. 1997. Leaf Form and Photosynthesis: Do leaf structure and orientation interact to regulate internallight and carbon dioxide? Bioscience, Washington, v. 47,p. 785-793.
Souza, V.C. & Lorenzi, H. Botânica sistemática: guia ilustrado para identificação das famílias de fanerógamas nativas e exóticas no Brasil, baseado na APG II. Nova Odessa. 2ª ed. Instituto Plantarum,. 2008.704p.
Taiz, L.; Zeiger, E. 2002. Plant Physiology. Sinauer Associates, Sunderland, MA, USA. 690pp.
Vidal, W.N & Vidal, M.R.R. Botânica Organografia – Quadros sinóticos ilustrados de fanerógamas. Viçosa: Universidade Federal de Viçosa. Ed. UFV. 2000. 124p.
Contato
Equipe executora da proposta:
Ioni Gonçalves Colares, é Oceanóloga, Doutora em Oceanografia Biológica (FURG), Mestre em Ciências Biológicas - Ecologia (INPA), dmbioni@furg.br
Sonia Marisa Hefler, é bióloga, Doutora em Botânica - Taxonomia Vegetal (UFRGS), Mestre em Botânica - Taxonomia Vegetal (UFPR), soniahefler@furg.br
Claudete Miranda Abreu, é bióloga, Doutora em Ciências Agrárias, Mestre em Fisologia Vegetal, claudeteabreu@furg.br
BolsistasTutores:
Kelen Veiga, é Bióloga, mestranda do curso de Biologia de Ambientes Aquáticos Continentais, krv.bio@gmail.com
André Jardim, é Bacharel em Ciência da Computação (UCPel), Mestre em Ciência da Computação (UCPel), adjardim@terra.com.br
Para falar conosco:
Universidade Federal do Rio Grande - FURG
Brasil, Rio Grande do Sul
Campus Carreiros: Rio grande, Av. Itália km 8 Bairro Carreiros - Fone (53)3233.6500 / (53)3233.8600
Campus Cidade: Rio Grande, Rua Alfredo Huch 475 Centro
Campus Saúde: Rio Grande, Rua Visconde de Paranaguá 102 Centro - Fone (53)3233.8800
Rio Grande CEP único: 96203-900
Campus Santa Vitória do Palmar: Rua Glicério P. de Carvalho, nº 81 Bairro Coxilha Cep 96230-000 - Fone (53) 3263.6500
Campus Santo Antônio da Patrulha: Barão do Caí, 125 Cidade Alta CEP: 95500-000 - Fone (51) 3662.6206
Campus São Lourenço do Sul: Rua Marechal Floriano Peixoto, 2236 Centro CEP 96170-000 - Fone (53) 3251.3933
Onde estamos:
Experimento 01
Hormônio - Etileno

Os hormônios vegetais são substâncias orgânicas que desempenham uma importante função na regulação do crescimento. O gás etileno, sintetizado a partir da metionina, na região do periciclo, é o único hidrocarboneto com efeito pronunciado sobre as plantas. Sua biossíntese ocorre em muitos tecidos em resposta ao estresse, especialmente em tecidos submetidos à senescência ou amadurecimento. Ele pode ser produzido por todas as partes das plantas superiores e sua taxa de produção dependente do tipo de tecido e do estágio de desenvolvimento.
Os tecidos vegetais convertem o 1-[14C]metionina em [14C]etileno, sendo o etileno derivado dos carbonos 3 e 4 da metionina. O grupo CH3-S da metionina é reciclado pelo ciclo de Yang, pois sem tal reciclagem, a quantidade de enxofre reduzida limitaria a disponibilidade de metionina e a síntese de etileno. A S-adenosilmetionina (AdoMet) é um intermediário na rota de biossíntese do etileno e o precursor imediato deste hormônio é o ácido 1-aminociclopropano-1-carboxílico (ACC).
Em geral, quando o ACC é suplementado de forma exógena ao tecido vegetal, a produção do etileno aumenta de maneira substancial, indicando que a síntese do ACC é em geral a etapa biosintética que limita a produção do etileno nos tecidos vegetais. A catalisação do etileno é realizada pelas enzimas ACC sintase e ACC oxidase. A ACC sintase é responsável pela a conversão do S-adenosilmetionina e é caracterizada em muitos tipos de tecidos de várias plantas. A ACC oxidase catalisa a última etapa na síntese do etileno: a conversão do ACC em etileno. Em tecidos que apresentam altas taxas de produção de etileno, como frutos em amadurecimento, a atividade da ACC oxidase pode ser o fator limitante na etapa de síntese.
A síntese do etileno é estimulada por vários fatores que vão desde o estágio de desenvolvimento da planta, condições ambientais, outros hormônios vegetais até lesões físicas e químicas. A biossíntese do etileno também varia de maneira circadiana, ocorrendo picos durante o dia e atingindo o mínimo durante a noite.
O gás etileno é ativo mesmo em concentrações muito baixas e pode causar efeito no amadurecimento de frutos, germinação de sementes, expansão e diferenciação celular, florescimento, senescência das folhas e flores, abscisão das folhas e frutos. A exposição de plântulas de algumas espécies a este gás provoca o crescimento horizontal dos caules.
O amadurecimento dos frutos envolve numerosas transformações. Sob uma perspectiva da planta, o amadurecimento do fruto indica que as sementes estão prontas para a dispersão, tanto com recursos mecânicos quanto com qualquer outro método dispersivo, tendo como resultado a desidratação e abertura de sementes.
O termo amadurecimento de frutos pode ainda referir-se a mudanças no fruto que o tornam pronto para ser consumido. Quando o fruto amadurece, a taxa do ACC e a biossíntese do etileno aumentam. A atividade enzimática, das enzimas ACC oxidase e ACC sintase é aumentada, bem como os níveis de mRNA de subgrupos gênicos codificadores de cada enzima.
Nos frutos carnosos, a clorofila é degradada e outros pigmentos podem formar-se alterando sua coloração. Simultaneamente, a parte carnosa do fruto amolece como resultado da digestão enzimática da pectina, o componente principal da lamela média da parede celular. Durante esse mesmo período o amido, ácidos orgânicos e óleos são metabolizados em açúcares. Há ainda o desaparecimento de ácidos orgânicos e de compostos fenólicos, incluindo os taninos. Como consequência dessas transformações, os frutos tornam-se visíveis, saborosos. Essas características podem frequentemente ser atribuídas ao acumulo de antocioninas e carotenoides na epiderme desses frutos, o que os tornam atrativos para os animais que se alimentam dos frutos e então disseminam as sementes. Porém, a avaliação de um grande número de frutos tem demonstrado que nem todos respondem ao etileno.
Todos os frutos que amadurecem em resposta ao etileno exibem, antes da fase de amadurecimento, um aumento característico da respiração celular, chamado de climatério. Tais frutos também apresentam um pico na produção do etileno, imediatamente antes do aumento da respiração. Maçãs, bananas, abacates e tomates são exemplos de frutos climatéricos. Em contraste, frutos cítricos e uvas não exibem aumento na respiração e na produção do etileno e são chamados de não climatéricos.
Quando frutos não-maduros e climatéricos são tratados com etileno, o início do climatério é acelerado. Quando frutos não-climatéricos são tratados da mesma forma, a magnitude do aumento respiratório ocorre em função da concentração do etileno, porém o tratamento não desencadeia a produção endógena do etileno nem acelera o amadurecimento.
O etileno tem sua síntese aumentada quando as plantas estão sob condições estressantes, como seca, inundação, resfriamento e exposição ao ozônio. O aumento na sua produção resulta, em parte, de um aumento na transcrição do mRNA da ACC sintase. Esse “etileno de estresse” está envolvido no inicio da resposta ao estresse, como, por exemplo, a abscisão foliar, senescência, regeneração de lesões e aumento na resistência a moléstias. A senescência foliar é um processo geneticamente programado que afeta todos os tecidos do vegetal e tem sua taxa aumentada devido ao etileno. O aumento na produção do etileno está associado à perda da clorofila e o desaparecimento gradual da cor, que são aspectos característicos da senescência das folhas e flores.
O uso de inibidores de síntese ou ação de hormônios são úteis para o estudo das rotas biosintéticas assim como dos papeis fisiológicos de tais substâncias. Os inibidores são principalmente úteis nos casos em que é difícil distinguir entre diferentes hormônios que apresentam efeitos idênticos nos tecidos vegetais ou quando um hormônio afeta a síntese ou a ação de outro hormônio.
Por exemplo, o etileno mimetiza altas concentrações de auxina (composto que induz a formação do etileno através do aumento da atividade da ACC sintase), provocando a epinastia (curvatura das folhas para baixo) e a inibição do crescimento do caule. A utilização de inibidores da biossíntese e da ação do etileno possibilita distinguir entre as ações das auxinas e do etileno. Os estudos utilizando inibidores mostram que o etileno é o agente primário da epinastia e que a auxina age indiretamente, causando um aumento substancial na produção do etileno. Algumas respostas atribuídas anteriormente à auxina na verdade devem-se à produção do etileno em resposta à auxina. Provavelmente essa atribuição errônea se dê ao fato de, em alguns casos, as respostas provocadas nas plantas, tanto pelo etileno quanto pela auxina serem semelhantes.
Vídeo - Formação do etileno em frutos climatéricos
Roteiro experimentação Etileno
OBJETIVO: Verificar a formação do etileno em frutos climatéricos
MATERIAL: 15 bananas no mesmo estágio inicial de “amadurecimento”; 15 laranjas no mesmo estágio inicial de “amadurecimento”; 4 maçãs maduras; 4 embalagens de plástico; 4 embalagens de papel; fita crepe para vedar as embalagens; geladeira.
PROCEDIMENTOS:
1) Deixe três bananas e três laranjas em temperatura ambiente que serão utilizadas como controle;
2) Coloque três bananas e uma maçã numa embalagem plástica, três bananas e uma maçã numa embalagem de papel, três laranjas e uma maçã em outra embalagem plástica e três laranjas e uma maçã numa outra embalagem de papel. Vede com fita crepe as quatro embalagens e coloque-as na geladeira.
3) Repita o procedimento acima mantendo as embalagens em temperatura ambiente (caso seja possível a temperatura ambiente poderá ser simulada em uma câmara de germinação com o objetivo de evitar grandes mudanças de temperatura).
É importante utilizar embalagens padronizadas e verificar se as mesmas não possuem orifícios.
4) Observe após 4 dias.
Responder:
Comparando as embalagens com a exposição ao ambiente, em qual ocorreu maior amadurecimento?
O que levou a serem diferentes?
Experimento 02
Gutação

Allium cepa - Foto do processo de gutação em plântula de capim-annoni (Eragrostis plana Ness.)
Foto: Claudete Abreu
O acumulo de solutos no xilema pode gerar a pressão de raiz. As raízes geram pressão hidrostática positiva absorvendo íons da solução diluída do solo e os transportam para o xilema. O acúmulo de solutos na seiva do xilema leva a um decréscimo no potencial osmótico (Ψs) e no potencial hídrico (Ψw) do xilema, que proporciona a força propulsora para a absorção de água, gerando uma pressão hidrostática positiva. A pressão da raiz tem maior ocorrência quando os potenciais hídricos do solo são altos e as taxas de transpiração são baixas. Quando as taxas de transpiração são altas, a água é rapidamente absorvida pelas folhas e perdida para a atmosfera e uma pressão positiva acaba nunca se desenvolvendo no xilema. As plantas que desenvolvem pressão na raiz frequentemente produzem gotículas líquidas nas margens de suas folhas, um fenômeno conhecido como gutação. A pressão positiva no xilema provoca a saída da seiva do xilema pelos poros presentes na epiderme das folhas denominados hidatódios. O soluto passa através dos espaços intercelulares do parênquima do hidatódio indo para o exterior através de poros especiais (estomas) que permanecem sempre abertos.
As “gotas de orvalho”, que podem ser vistas sobre a lâmina foliar de gramíneas e ao longo da margem de algumas folhas de plantas herbáceas pela manhã, são na verdade gotículas de gutação exsudadas dos estomas. A gutação é mais perceptível quando a transpiração é suprimida e a umidade relativa do ar e do solo é alta, o que geralmente ocorre durante a noite
Roteiro experimentação Gutação
Objetivo: Observar a gutação em plantas jovens de milho.
Material: 3 plantas jovens de milho, água quente, água a 0°C, termômetro, béquer grande
Procedimento:
Regar cada vaso, etiquetando com: solo seco; água quente; água 0°C.
Cobrir cada planta com o béquer grande.
Observar o comportamento de cada planta.
Responder:
Qual das plantas realizou gutação?
Em qual região da folha foi observada a gutação?
Experimento 03
Plasmólise

Plasmólise é a condição em que o protoplasto se desprende da parede celular, devido à saída de água do protoplasto por osmose; essencialmente é um fenômeno de laboratório, com possíveis exceções em condições extremas de estresse salino ou de água, que raramente ocorrem na natureza. As células vegetais acumulam em seus vacúolos soluções relativamente concentradas em sais, e também podem acumular açúcares, ácidos orgânicos e aminoácidos. Uma das consequências é o aumento da pressão hidrostática no interior das células devido à entrada constante dá agua por osmose. Essa pressão contra a parede celular mantém a célula turgida. Consequentemente, a pressão hidrostática em uma célula vegetal é geralmente referida como a pressão de turgor que é definida como a pressão que se desenvolve no interior de uma célula vegetal como resultado da osmose e/ou embebição. Igual e oposta à pressão de turgor em qualquer momento é a pressão mecânica da parede celular, dirigida para o interior da célula, chamada de pressão da parede.
O turgor em um vegetal é especialmente importante como suporte para as regiões não-lenhosas de uma planta. Quase todo o crescimento de uma célula vegetal resulta da absorção de água, com a maior parte do aumento em tamanho da célula resultante do aumento de tamanho dos vacúolos. O turgor é mantido nas células vegetais porque a maioria das células existe em meios com potencial hídrico relativamente elevado.
Por outro lado, se uma célula vegetal é colocada em uma solução com potencial hídrico relativamente baixo, a água então sairá da célula por osmose, e o vacúolo e protoplasto irão se retrair, desse modo a membrana será afastada da parede celular. O processo pode ser revertido se, em seguida, a célula for transferida para a água pura. A partir desses processos é possível determinar a turgidez da célula, assim como as taxas de soluto que estão atravessando a membrana celular.
Vídeo - Plasmólise
Roteiro experimentação Plasmólise
OBJETIVO: Verificar a ocorrência de plasmólise
MATERIAL: placas de Petri, água destilada soluções de sacarose (0,3M, 0,4M, 0,5M, 0,6M, 0,7M, 0,8M, 0,9M, 1,0M), epiderme inferior de folha de Zebrina pendula, microscópio, laminas, lamínulas.
PROCEDIMENTOS:
1) Coloque 20ml de agua destilada em uma das placas e nas demais as concentrações de sacarose correspondente, mantenhas as placas tampadas;
2) Coloque em cada uma das placas 2 a 3 pedaços de epiderme inferior de folha de Zebrina pendula
3) Após cinco minutos monte uma lamina com lamínula com todas as concentrações iniciando pela agua destilada e observe no microscópio e desenhe
4) Determine em quais concentrações pode ser observada a plasmólise.
Responder:
Em quais concentrações houve a plasmólise?
Qual o processo que ocorreu?
Experimento 04
Geotropismo

Tropismo é uma resposta de crescimento envolvendo a curvatura de uma parte de uma planta na mesma direção (positiva) ou em direção oposta (negativa) a um estimulo externo. O geotropismo, ou gravitropismo é o crescimento em resposta à gravidade. Os amiloplastos (estatólitos), presentes em muitas células vegetais, servem como sensores à gravidade. As células especializadas em perceber o estímulo gravitacional nas quais eles ocorrem são chamadas estatócitos.
Se uma plântula é colocada na posição horizontal, suas raízes crescerão para baixo (geotropismo positivo) e seu sistema caulinar crescerá para cima (geotropismo negativo), comportamento é extremamente crítico nos estágios iniciais de germinação. Isso se deve ao fato de as raízes serem mais sensíveis a auxina do que os caules, e em altas concentrações de auxina, o crescimento das raízes é inibido.
Os tecidos abaixo do ápice também são capazes de responder à gravidade. Ao contrario da luz unilateral, a gravidade não forma um gradiente entre as metades inferiores e superiores de um órgão. Todas as partes da planta percebem igualmente um estimulo gravitacional. A parte inferior do caule colocado na posição horizontal é estimulada pela auxina e cresce mais rapidamente do que o respectivo lado superior. O resultado disso é uma curvatura dos caules para cima. Para a raiz, o nível relativamente elevado de auxina no lado inferior inibe o crescimento, ocasionando assim o encurvamento deste órgão para baixo.
Roteiro experimentação geotropismo
OBJETIVO: Observar o movimento da planta em direção a luz
MATERIAL: Planta envasada de crescimento rápido (feijão, batata, etc)
PROCEDIMENTOS:
1) Escolha uma planta que esteja na fase vegetativa e deixe o vaso de modo que a planta fique na posição horizontal. Mantenha o substrato umedecido.
2) Coloque o vaso em câmara escura.
3) Observe diariamente durante uma semana o que esta ocorrendo, marque em folha de papel as curvaturas que a planta seguiu.
Responder:
O que foi observado com o ângulo da planta?
Como você explica o que observou?
Por que o experimento foi realizado no escuro?
Experimento 05
Pigmentos (Clorofila)

Um pigmento é qualquer substância que absorve luz visível. Alguns pigmentos absorvem todos os comprimentos de onda da luz e, portanto, apresentam-se negros. Entretanto, a maior parte absorve apenas certos comprimentos de onda, transmitindo ou refletindo os comprimentos de onda não absorvidos. A clorofila é o pigmento que confere a cor verde às folhas. Isso ocorre devido a sua absorção principalmente de luz nos comprimentos de onda violeta e azul bem como no vermelho. A absorção da luz azul excita a clorofila a um estado energético mais elevado que a absorção de luz vermelha, pois a energia dos fótons é maior quando seus comprimentos de onda são menores.
Uma evidência de que a clorofila é o principal pigmento envolvido na fotossíntese é a similaridade entre o espectro de absorção e o espectro de ação da fotossíntese. No estado excitado, a clorofila é extremamente instável e rapidamente libera parte de sua energia ao meio como calor, entrando em um estado de menor excitação de alguns nanossegundos. No estado de menor excitação, a clorofila excitada libera energia como calor, como fluorescência, como transferência de energia ou provocando a ocorrência de reações químicas (processo fotoquímico). A luz é absorvida, principalmente pelos complexos-antena, os quais são compostos por clorofilas, pigmentos acessórios e proteínas, estando localizados nas membranas dos tilacóides dos cloroplastos.
Os centros de reação, que contém complexos proteicos com muitas subunidades e uma quantidade massiva de clorofila, iniciam uma série de reações químicas complexas que capturam energia na forma de ligações químicas. A energia da luz solar é primeiramente absorvida pelos pigmentos da planta. Todos os pigmentos ativos no processo de fotossíntese são encontrados nos cloroplastos. As clorofilas e as bacterioclorofilas (pigmentos encontrados em algumas bactérias) são os pigmentos típicos dos organismos fotossintéticos, mas todos os organismos possuem uma mistura de mais de um tipo de pigmento, cada um desempenhando uma função específica. As clorofilas a e b são abundantes nas plantas verdes, e as c e d são encontradas em alguns protistas e cianobactérias.
Os carotenoides são encontrados nos organismos fotossintéticos, e constituem integralmente as membranas dos tilacoides e estão, em geral, intimamente associados aos pigmentos protéicos das antenas e dos centros de reação. A luz absorvida pelos carotenóides é transferida à clorofila para o processo de fotossíntese e em decorrência do papel que desempenham são chamados de pigmentos acessórios.
Vídeo - Propriedade das Clorofilas
Roteiro experimentação pigmentos
Separação dos Pigmentos Vegetais Foliares por Cromatografia de Papel
Objetivo: Identificar qualitativamente os pigmentos obtidos do extrato orgânico de folhas verdes.
Material:Folhas verdes de espinafre, papel alumínio, gral com pistilo, funil, provetas, béquer, pipetas, papel filtro, bastão de vidro, durex, papel cromatográfico Whatmann n° 1, Reagentes: acetona, álcool etílico, éter de petróleo
Procedimento:
1) Preparar 60 ml, numa proporção de 1:1:1, de éter de petróleo, acetona e etanol.
2) Macerar algumas folhas de espinafre.
3) Adicionar o solvente.
4) Retirar o extrato de pigmentos, colocando na cuba cromatográfica.
5) Colocar uma tira de papel cromatográfico dentro da cuba em contato com o extrato.
6) Esperar algum tempo para observar.
Propriedade das Clorofilas
Objetivo: Demonstrar algumas propriedades das clorofilas.
Material:Folhas verdes de espinafre, tubos de ensaio e suportes, gral com pistilo, etiquetas, provetas, pipetas, funil, papel filtro, Reagentes: álcool etílico, água oxigenada, benzina e ácido acético.
Procedimento:
1) Macerar algumas folhas de espinafre e acrescentar ao macerado 40 ml de álcool.
2) Filtrar.
3) Transferir o filtrado para 4 tubos de ensaio (manter a mesma quantidade nos tubos).
4) Observar:
Tubo 1 : controle. Observar fluorescência (Só com bastante luz solar).
Tubo 2: adicionar 2 ml de ácido acético. Observar feofitinas.
Tubo 3 : adicionar 4 ml de água oxigenada. Observar oxigenação.
Tubo 4 : adicionar 6 ml de benzina. Observar a separação dos pigmentos.
Experimento 06
Fotoperiodismo

O fotoperíodo é o comprimento relativo do dia e da noite. Já o fotoperiodismo representa a habilidade de um organismo, em detectar e responder às variações do comprimento dos dias, ou seja, é uma resposta biológica a uma mudança nas proporções de luz e escuro num ciclo diário de 24horas.
As respostas das plantas controladas pelo comprimento do dia são numerosas, incluindo a iniciação do florescimento, a reprodução assexual, a formação de órgãos de reserva e a indução de dormência. Talvez todas as respostas fotoperiódicas das plantas utilizem os mesmos fotorreceptores, com rotas de transdução de sinais subsequentes especificas que regulam respostas diferentes.
A classificação das plantas de acordo com suas respostas fotoperiódicas está baseada no florescimento, embora muitos outros aspectos do desenvolvimento das plantas possam também ser afetados pelo comprimento do dia. Elas podem ser agrupadas em três tipos gerais, plantas de dias longos, plantas de dias curtos e plantas neutras. A distinção essencial entre as plantas é que o florescimento nas plantas de dias longos é estimulado somente quando o comprimento do dia excede uma certa duração, chamada de comprimento crítico do dia, em cada ciclo de 24 horas, enquanto a estimulação do florescimento nas plantas de dias curtos requer um comprimento de dia menor do que o comprimento critico do dia. O valor do comprimento crítico do dia varia amplamente entre as espécies.
As plantas de dias longos florescem somente em dias em que o período de luz for mais longo ou tem florescimento acelerado por dias longos. Estas tem ocorrência principalmente no verão. Por muitos anos, os fisiologistas vegetais acreditaram que a correlação entre os dias longos e o florescimento era uma consequência da acumulação de produtos da fotossíntese sintetizados durante aqueles dias. As plantas de dias curtos florescem apenas em dias curtos, ou tem florescimento acelerado por dias curtos. São características do início da primavera ou outono, pois passam por um período de luz menor do que um comprimento crítico. Tem-se ainda as plantas de dias neutros, que florescem independentemente da condição de fotoperíodo, são insensíveis ao comprimento do dia. Seu florescimento está tipicamente sob regulação autônoma, isto é, controle do desenvolvimento interno.
O fator mais importante para o desenvolvimento de uma planta não é o comprimento absoluto do fotoperíodo, mas sim se este é mais longo ou curto do que um certo intervalo crítico. As plantas exibem várias adaptações para evitar a ambiguidade do sinal do comprimento do dia. Uma delas é a ligação da exigência de temperatura a uma resposta fotoperiódica. Certas espécies de plantas não respondem ao fotoperíodo, até que tenha ocorrido um período de frio.
Sob condições naturais, os comprimentos do dia e da noite configuram um ciclo de 24 horas de luz e escuro. Em princípio, uma planta poderia perceber um comprimento crítico do dia pela medição da duração tanto da luz quanto do escuro. É possível induzir o florescimento nessas plantas com períodos de luz mais longos do que o valor crítico, desde que os mesmos sejam seguidos por noites suficientemente longas. Da mesma forma, tais plantas não florescem quando dias curtos são seguidos por noites curtas, após tal indução. As plantas de dias longos florescem em dias curtos, desde que o comprimento da noite seja também curto, por indução. Contudo, um regime de dias longos seguidos por noites longas não surge efeito em tais plantas induzidas.
O período de escuro pode se tornar não efetivo pela interrupção com uma curta exposição à luz, chamada de quebra da noite. Por outro lado, a interrupção de um dia longo com um breve período de escuro não cancela o efeito do dia longo. Tratamentos de quebra da noite de apenas poucos minutos são efetivos no impedimento do florescimento de muitas espécies de dias curtos, mas exposições muito mais longas são necessárias para promover o florescimento em plantas de dias longos
Roteiro experimentação fotoperiodismo
OBJETIVO: Discutir eventos fisiológicos influenciados pela luz
MATERIAL: Sementes de feijão e milho, potes de plástico, areia lavada.
PROCEDIMENTOS:
1) Coloque 5 sementes de feijão em cada pote contendo areia lavada com no mínimo oito repetições.
2) Mantenha quatro potes em luz plena e os outros no escuro total.
3) Repita o mesmo procedimento com as sementes de milho.
4) Observar após cinco das o efeito da luz (presença e ausência) sobre o desenvolvimento das plântulas, destacando a mudança no padrão do desenvolvimento.
5) Elaborar uma tabela comparando as plântulas de feijão crescidas na presença e ausência de luz , o mesmo deverá ser feito com as plântulas de milho.
|
Características observadas |
Feijão |
Milho |
||
|
Escuro |
Luz |
Escuro |
Luz |
|
|
Pigmentação |
|
|
|
|
|
Rigidez caulinar |
|
|
|
|
|
Sistema radicular |
|
|
|
|
|
Folhas primárias |
|
|
|
|
|
|
|
|
|
|
|
Comprimento do hipocótilo |
|
|
|
|
|
Comprimento do epicótilo |
|
|
|
|
|
Gancho plumular |
|
|
|
|
|
Comprimento do mesocótilo |
|
|
|
|
|
Comprimento do coleópitile |
|
|
|
|
Experimento 07
Germinação
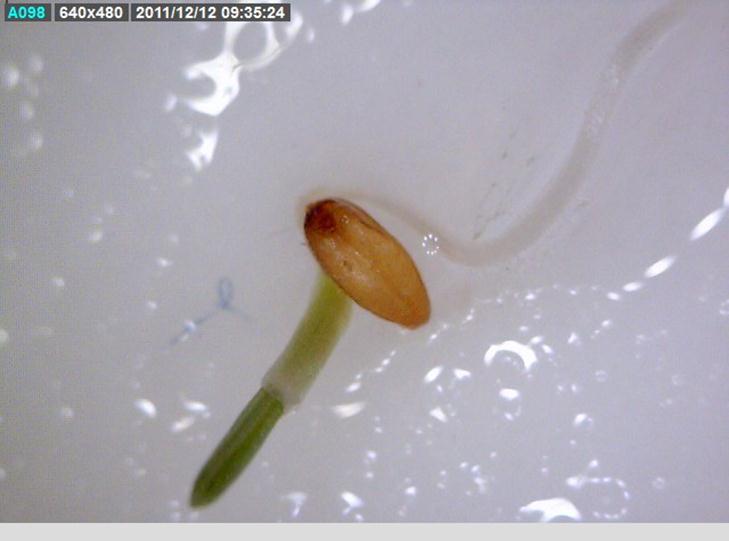
A palavra germinação refere-se ao conjunto de processos associados à fase inicial ou de retomada do crescimento de uma estrutura da planta. O crescimento do embrião é o mesmo que a germinação da semente. Durante a fase inicial do processo de desenvolvimento, que inicia com a entrada de água na semente (embebição), o metabolismo será ativado, e quando há o rompimento do tegumento, a respiração que até então era anaeróbica passa a ser aeróbica, requerendo oxigênio. De acordo com o critério fisiológico, a germinação é completa quando uma parte do embrião, em geral a radícula, penetra e trespassa os tecidos que o envolvem.
As sementes normalmente germinam no solo em ausência de luz. Se as sementes são germinadas no escuro, os proplastídeos se diferenciam em estioplastos, os quais apresentam arranjos semicristalinos tubulares de membranas conhecidos como corpos pró-lamelares. Em vez da clorofila, os estioplástos contém um pigmento precursor, de cor verde-amarelada, o protoclorofilida.
Embora muitas sementes germinem dentro de uma ampla faixa de temperatura, elas geralmente não germinarão abaixo ou acima de uma certa faixa específica de temperatura para a espécie. Algumas não germinam mesmo quando as condições externas são favoráveis, sendo chamadas dormentes. Essa dormência pode muitas vezes ser quebrada pela aplicação de giberelina (grupo de hormônios associados à promoção do crescimento do caule). Visto que as mudanças nos níveis de giberelinas são frequentemente, mas não sempre, observadas em resposta ao resfriamento, elas podem representar um regulador natural de um ou mais processos envolvidos na germinação entre elas: a ativação do crescimento vegetativo do embrião, o enfraquecimentro da camada do endosperma que envolve o embrião e restringe seu crescimento e a mobilização das reservas energéticas do endosperma.
Cada espécie de semente tem um certo período de viabilidade. Algumas espécies possuem sementes que precisam germinar no máximo duas semanas após sua dispersão. Outras (gênero Lótus) são conhecidas por terem até 2000 anos de idade e ainda serem capazes de germinar. No caso de uma semente ainda ser viável, o embrião dentro dela necessita algo para que seu metabolismo se mantenha ativo e inicie o processo de crescimento.
Vídeo - Germinação de Capim-annoni (Eragrostis plana Ness)
Roteiro experimentação germinação
OBJETIVO: Observar o efeito da temperatura em diferentes espécies
MATERIAL: Sementes de feijão, milho, alface, ervilha, caixas tipo Gerbox® ou placas de Petri, papel para germinação, germinador, água destilada.
PROCEDIMENTOS:
1) Prepare dois lotes de sementes de cada espécie com no mínimo quatro repetições, submetendo-as ao seguintes tratamento: 10 lote coloque em temperatura ambiente registrando a temperatura diariamente, 20 lote submeta a temperaturas diferentes variando de 100C a 300C.
2) Coloque as sementes conforme as Regras de Analise de Sementes (RAS) e mantenha de acordo com o tratamento.
3) Observe a germinação seguindo a RAS.
Experimento 08
Nutrição

Além de luz, as plantas necessitam de água e certos elementos químicos para o metabolismo e crescimento. Ao contrário do que ocorre com os animais, a demanda nutricional das plantas é relativamente simples. Sob condições ambientais favoráveis, a maioria das plantas verdes pode usar a energia luminosa para transformar CO2 e H2O em compostos orgânicos usados como fonte de energia. Elas também podem sintetizar todos os seus aminoácidos e vitaminas usando nutrientes inorgânicos extraídos do ambiente.
A nutrição das plantas envolve a absorção de todos os materiais brutos do ambiente necessários para os processos bioquímicos essenciais à distribuição desses materiais dentro da planta e à sua utilização no metabolismo e crescimento. Foi estabelecido que pelo menos 10 dos elementos químicos presentes nas plantas são essenciais para o crescimento normal. Um elemento essencial é definido como aquele cuja ausência impede uma planta de completar seu ciclo de vida, quando este elemento é específico e não pode ser substituído e ainda quando está envolvido diretamente no metabolismo da planta, fazendo parte de um constituinte essencial (por exemplo, uma enzima) ou exigido para um passo metabólico específico (por exemplo, numa reação enzimática).
Se as plantas recebem esses elementos, assim como energia da luz solar, elas podem sintetizar todos os compostos de que necessitam para um crescimento normal. Na ausência de qualquer desses elementos, as plantas podem exibir anomalias características de crescimento ou sintomas de deficiência, além da não reprodução normal dessas plantas. Quando os sintomas de deficiência aguda são relacionados a um elemento essencial em particular, uma pista importante é a extensão em que um elemento pode ser reciclado de folhas mais velhas para folhas mais jovens. Se um elemento essencial é móvel, sintomas da deficiência tendem a aparecer primeiro nas folhas mais velhas. A deficiência de um elemento essencial imóvel vai tornar-se evidente primeiro em folhas mais jovens.
A concentração de elementos específicos nas plantas varia numa ampla faixa. As necessidades de elementos minerais mudam ao longo do crescimento e do desenvolvimento de uma planta. Com base na concentração usual nas plantas, os nutrientes essenciais podem ser divididos em: macronutrientes, que são elementos necessários em grandes quantidades (potássio, nitrogênio, fósforo) e micronutrientes, ou elementos-traço, que são necessários em pouca quantidade (ferro, cloro, cobre, zinco).
Alguns pesquisadores propuseram a classificação dos elementos essenciais de acordo com seu papel bioquímico e sua função fisiológica, dividindo-se em quatro grupos:
O primeiro, formado pelos compostos orgânicos (com C) das plantas. As plantas assimilam esses nutrientes por meio de reações bioquímicas envolvendo oxidações e reduções. O segundo, importante em reações de armazenagem de energia ou manutenção da integridade estrutural. Os elementos deste grupo estão comumente presentes em tecidos vegetais sob forma de fosfato, borato e ésteres silicato, em que o grupo alimentar está ligado ao grupo hidroxila de uma molécula orgânica. O terceiro, presente no tecido vegetal como íons livres ou ligados a substâncias tais como ácidos pécticos, presentes na parede celular vegetal. Apresentam importância por aturarem como cofatores enzimáticos e na regulação de potenciais osmóticos. E o quarto, que desempenha importantes funções em reações envolvendo transporte de elétrons.
Vídeo - Nutrição Vegetal: desenvolvimento de plântulas com diferentes soluções nutritivas
Roteiro experimentação nutrição
Objetivo: Observar o desenvolvimento de plantas sob diferentes deficiências nutritivas.
Material: sementes de tomate / milho, areia lavada com água destilada, vasos plásticos com perfurações na base, soluções nutritivas de Clark
Procedimento:
Colocar as sementes para germinar nos vasos com areia. Ao emergir as plântulas, começar a irrigação, considerando os seguintes tratamentos:
a) solução nutritiva completa
b) solução nutritiva sem nitrogênio
c) solução nutritiva sem fósforo
d) solução nutritiva sem potássio
** A irrigação com as diferentes soluções nutritivas deverá ser feita duas vezes por semana, colocando água destilada entre os intervalos, quando o solo apresentar-se muito seco.
Ao final de aproximadamente 60 dias, observar o desenvolvimento das plantas mantidas com cada tratamento. Observar o aparecimento de alterações morfológicas nas plantas sob deficiência nutricional, relacionando-os com aspectos fisiológicos.
Responder:
a) Qual o aspecto das plantas sob deficiência de nitrogênio, fósforo ou potássio?
b) Como ocorreu o crescimento das plantas?
c) Compare as características das plantas com diferentes tratamentos, observando: altura da planta, tamanho e número das folhas, coloração, tamanho das raízes ou o seu volume, entre outras.
d) Explique, com base na fisiologia, as alterações que ocorreram nas plantas sob deficiência de N, P ou K, qual a importância destes elementos no crescimento e desenvolvimento da planta.
e) Explique porque não houve necessidade de colocar a solução nutritiva durante a germinação das sementes? Como as plântulas desenvolveram-se sem a necessidade de adubação?
ETAPAS GERAIS: semeadura em vasos plásticos com areia lavada e preparo da solução nutritiva.
|
Solução |
PM |
Estoque |
g/litro p/estoque |
Volume em ml para 1 litro |
|
MgCl2 6H2 O |
203,2 |
1M |
203,2 |
1,0 |
|
Ca(NO3 )2 4H2 O |
236,08 |
1M |
236,08 |
2,6 |
|
NH4 NO3 |
80 |
1M |
80 |
1,0 |
|
KCl |
74,55 |
1M |
74,55 |
1,0 |
|
MgSO4 7H2 O |
246,36 |
0,5M |
123,18 |
1,0 |
|
KH2 PO4 |
136,07 |
0,07M |
9,52 |
3,0 |
|
Micronutrientes |
|
|
|
1,0 |
|
Fe-EDTA |
|
|
|
0,5 |
Experimento 09
Amido

É o principal carboidrato de reserva energética das plantas. É estável e insolúvel e está presente em quase todas as plantas. Nas células vegetais, o amido é armazenado na forma de grânulos insolúveis em água. No caso das folhas, é sintetizado e armazenado nos cromoplastos ou nos amiloplastos, a partir da polimerização da glicose, resultante da fotossíntese.
Nos cloroplastos, o amido é sintetizado a partir da triose fosfato gerada pelo ciclo de Calvin, durante o período fotossintético, sendo rapidamente metabolizado durante o período noturno. Os amiloplastos são encontrados em vários tecidos e órgãos não fotossintetizantes, como parênquima de raízes e caules, tubérculos, endosperma ou cotilédones de sementes.
Vídeo - Presença de Amido de folhas variegadas de Coleus sp.
Roteiro experimentação amido
OBJETIVO: Detectar a presença de amido nas folhas
MATERIAL: Folhas de Coleus sp., béquer, placa de Petri, bastão de vidro, banho–maria, I2 (iodo), KI (iodeto de potássio), álcool etílico 80%, pinça
PROCEDIMENTOS:
1) Prepare um volume de 100ml utilizando 0,1g de iodo e 0,5g de iodeto de potássio diluído em 80ml de álcool etílico e 20ml de agua destilada (solução de Lugol)
2) Observe folha variegada onde se encontram as partes mais claras e desenhe.
3) Coloque a folha em água fervente até ficar clara (ausência de pigmentos).
4) Em outro béquer coloque álcool para que seja eliminada totalmente os pigmentos.
5) Coloque a folha em placa de Petri com água em temperatura ambiente a fim de hidratar.
6) Retire a folha coloque em outra placa e adicione a solução de Lugol.
7) Observe as parte mais escuras e compare com o desenho.
Responda:
Em quais partes da folha a cor marrom ficou mais intensa?
Por que ocorreu este processo?
Experimento 10
Xilema e Floema

O sistema vascular das plantas apresenta basicamente dois componentes: o floema, sistema pelo qual o alimento fabricado nas folhas ou outras regiões fotossintetizantes é transportado pelo vegetal e o xilema, através do qual a agua ascende pelo corpo da planta. Esse sistema de transporte originou o maior grupo vegetal, denominado plantas vasculares. As duas rotas de transporte de longa distância – o floema e o xilema – estendem-se por toda a planta
O floema é o principal tecido condutor de seiva elaborada das plantas vasculares. Esse tecido é, em geral, encontrado na face externa dos tecidos vasculares, primário e secundário. Nas plantas com crescimento secundário, o floema constitui a casca viva. É responsável por translocar os produtos da fotossíntese e das folhas maduras para as áreas de crescimento e armazenagem, incluindo as raízes. Ele também redistribui a água e os vários compostos através do corpo da planta. As células do floema que conduzem açúcares e outros compostos orgânicos através da planta são chamadas de elementos crivados. Em alguns casos, o tecido do floema também inclui fibras e esclereides. Porém apenas os elementos crivados estão envolvidos diretamente na translocação.
O xilema é um tecido vascular complexo por onde a maior parte da água e sais minerais são conduzidos a partir do sistema radicular até as partes aéreas dos vegetais. Trata-se do principal tecido condutor de água nas plantas vasculares e na maioria das plantas, constitui a porção mais longa da rota de transporte de água. É também envolvido na condução de minerais, substâncias de reserva e sustentação. Junto com o floema, o xilema forma um sistema continuo de tecido vascular que se estende pelo corpo da planta.
O xilema é caracterizado pela presença de elementos traqueais, suas principais células condutoras. As células condutoras tem uma anatomia especializada que lhes permite transportar grandes quantidades de água com grande eficiência. Existem dois tipos importantes de elementos traqueais no xilema: traqueídes e elementos de vaso. Elementos de vaso são encontrados somente em um pequeno grupo de angiospermas e talvez em algumas pteridófitas. Traqueídes estão presentes tanto em angiospermas quanto em gimnospermas, assim como em pteridófitas e outros grupos de plantas vasculares.
A maturação tanto de traqueídes quanto de elementos de vaso envolve a “morte” da célula. Assim, células condutoras de agua funcionais não tem membranas e organelas. O que permanece são paredes celulares lignificadas e grossas, que formam tubos ocos através dos quais a agua pode fluir com resistência relativamente baixa.
Em teoria, os gradientes necessários para mover agua por meio do xilema poderiam resultar da geração de pressões positivas na base da planta ou de pressões negativas no topo da planta. Algumas raízes podem desenvolver pressões hidrostáticas positivas em seus xilemas – a chamada pressão de raiz. Em vez disso, a água no topo de uma árvore desenvolve uma grande tensão (pressão hidrostática negativa), a qual puxa a água pelo xilema. Esse mecanismo é chamado de teoria coesão-tensão de ascensão da seiva, por requerer as propriedades de coesão da água para suportar grandes tensões nas colunas de agua do xilema.
O floema transporta metabolitos da parte aérea para a raiz e o xilema transporta água e solutos para a parte aérea. O floema desenvolve-se mais rapidamente que o xilema, evidenciando o fato de que a função do floema é crítica junto ao ápice radicular. Grandes quantidades de carboidratos devem fluir através do floema em direção às zonas apicais em crescimento, para sustentar a divisão e o alongamento celular. É na zona de maturação o local onde o xilema desenvolve a capacidade de transportar quantidades substanciais de água e solutos para a parte aérea.
Vídeo - Vasos de condução: Xilema e Floema
Roteiro experimentação xilema e floema
Objetivo: Observar a ascensão de diferentes soluções coradas em caule de Cucurbitaceae.
Material: 2 frascos erlenmeyer (ou béquer), solução de azul de metileno (0,1 %), solução de eosina (0,1 %), lâmina de barbear, água destilada, microscópio, caule de Cucurbitaceae.
Procedimento:
1) Colocar num erlenmeyer um pouco de solução de azul de metileno e no outro de eosina.
2) Cortar 2 pedaços do caule de Cucurbitaceae, aproximadamente 10 cm, colocando-os verticalmente na água destilada.
3) Corte longitudinalmente uma das extremidades de cada caule.
4) Coloque um dos caules no azul de metileno e o outro na eosina.
5) Observar a ascensão das soluções. Responda:
Qual das duas soluções sobe mais rapidamente?
Observação: Sabe-se que a celulose em contato com a água apresenta carga elétrica negativa (-) na sua superfície. O azul de metileno tem carga elétrica negativa (-) e a eosina carga elétrica positiva (+).
Considerando estes fatos, explique porque ocorre diferença de velocidade na ascensão das soluções usadas.
Faça cortes transversais e longitudinais nos caules utilizadas, e observe ao microscópio para comparação da ascensão.
Identifique os vasos condutores das soluções coradas (eosina e azul de metileno).
Fisiologia Vegetal
A fisiologia vegetal estuda os fenômenos vitais que acontecem nas plantas. Estes fenômenos podem referir-se ao metabolismo, desenvolvimento, crescimento e reprodução vegetal. Considerando-se que as plantas são organismos dinâmicos, em fisiologia vegetal estudamos todos os processos e estruturas que contribuem para a vida da planta.
A fisiologia vegetal se inter-relaciona com diversas áreas, entre elas: genética, bioquímica, física, química, biofísica, microbiologia.
Passe o mouse por sobre os experimentos listados e veja como reproduzi-los.
|
EXPERIMENTO 01: Hormônio - Etileno Os hormônios vegetais são substâncias orgânicas que desempenham uma importante função na regulação do crescimento. O hormônio etileno é um gás, cuja biossíntese ocorre em muitos tecidos em resposta ao estresse, especialmente em tecidos submetidos à senescência ou amadurecimento. |
|
O termo gutação é empregado para as gotículas líquidas presentes nas margens das folhas de plantas que desenvolvem pressão na raiz. A saída das gotículas líquidas ocorre através dos hidatódios. A gutação é mais perceptível quando a transpiração é suprimida e a umidade relativa do ar e do solo é alta, o que geralmente ocorre durante a noite. |
|
Plasmólise é a condição em que o protoplasto se desprende da parede celular, devido à saída de água do protoplasto por osmose. Este fenômeno é observado quando a célula vegetal é colocada em uma solução com potencial hídrico relativamente baixo. |
|
Geotropismo ou gravitropismo é o crescimento das plantas em resposta à gravidade. Os amiloplastos (estatólitos), presentes em muitas células vegetais, servem como sensores à gravidade. As células especializadas em perceber o estímulo gravitacional nas quais eles ocorrem são chamadas estatócitos. |
|
EXPERIMENTO 05: Pigmentos (Clorofila) A clorofila é o pigmento que ocorre em todos os organismos fotossintetizantes. A absorção de luz da clorofila ocorre nos comprimentos de onda violeta e azul bem como no vermelho. A absorção da luz azul excita a clorofila a um estado energético mais elevado que a absorção de luz vermelha, pois a energia dos fótons é maior quando seus comprimentos de onda são menores. |
|
EXPERIMENTO 06: Fotoperiodismo Fotoperiodismo representa uma resposta biológica a mudança nas proporções de luz e escuro num ciclo diário de 24horas. A classificação das plantas de acordo com suas respostas fotoperiódicas está baseada no florescimento, sendo agrupadas em três tipos gerais, plantas de dias longos, plantas de dias curtos e plantas neutras. |
|
Germinação refere-se ao conjunto de processos associados à fase inicial ou de retomada do crescimento de uma estrutura da planta. O crescimento do embrião é o mesmo que a germinação da semente. De acordo com o critério fisiológico, a germinação é completa quando uma parte do embrião, em geral a radícula, penetra e trespassa os tecidos que o envolvem. |
|
A nutrição vegetal envolve a absorção de todos os materiais necessários para os processos bioquímicos essenciais a serem utilizados no seu metabolismo e crescimento. Um elemento essencial é definido como aquele cuja ausência impede a planta de completar seu ciclo de vida, quando este elemento é específico e não pode ser substituído e ainda quando está envolvido diretamente no metabolismo da planta. |
|
Amido é o principal carboidrato de reserva energética das plantas. É armazenado nas células vegetais na forma de grânulos insolúveis em água. No caso das folhas, é sintetizado e armazenado nos cromoplastos ou nos amiloplastos, a partir da polimerização da glicose, resultante da fotossíntese. |
|
EXPERIMENTO 10: Xilema e Floema O xilema é um tecido vascular complexo por onde a maior parte da água e sais minerais são conduzidos, a partir do sistema radicular até as partes aéreas dos vegetais. O floema é o principal tecido condutor de seiva elaborada das plantas vasculares. É responsável por translocar os produtos da fotossíntese e das folhas maduras para as áreas de crescimento e armazenagem, incluindo as raízes. |
Introdução
O Instituto de Ciências Biológicas - ICB, da Universidade Federal do Rio Grande - FURG, tem como filosofia o incentivo e a realização de atividades de geração, integração e difusão de conhecimentos, bem como a formação e capacitação de recursos humanos em Ciências Biológicas.
Ciências Biológicas é uma grande área do conhecimento, representada por diversas matérias, entre elas a matéria Botânica. No prédio da Botânica, estão localizados os laboratórios onde os professores e técnicos administrativos em educação desenvolvem suas atividades.
Nestes laboratórios são desenvolvidos trabalhos de pesquisa dos alunos de diversos cursos de graduação e pós-graduação da FURG. Entre os cursos de graduação atendidos, temos: Arqueologia, Ciências Biológicas Bacharelado, Ciências Biológicas Licenciatura, Oceanologia e Tecnologia em Toxicologia Ambiental. Entre os cursos de pós-graduação atendidos, temos: o Mestrado Biologia de Ambientes Aquáticos Continentais e a Especialização em Diversidade Vegetal.
A matéria Botânica também presta acessoria a professores da rede municipal e estadual de ensino, pesquisadores de outras instituições e a comunidade em geral, através de permuta de informações e material do acervo pertencente ao Herbário HURG.
As linhas de pesquisa desenvolvidas nos laboratórios de Botânica envolvem as áreas de anatomia, morfologia, fisiologia e sistemática vegetal. Estas atividades envolvem professores, técnicos administrativos em educação, discentes de graduação e discentes de pós-graduação.
São professores da Botânica: profa. Dra. Claudia Giongo, profa. Dra. Claudete Miranda Abreu, prof. Dr. Danilo Giroldo, profa. Dra. Ioni Gonçalves Colares, profa. Dra. Luciana da Silva Canêz, profa. Dra. Sonia Marisa Hefler, prof. Dr. Ubiratã Jacobi.
Técnicos Administrativos em Educação: Caroline Igansi Duarte, Eonice Soares Lacerda, Guilherme Ceolin.
O principal objetivo deste site está em contribuir para a melhoria do ensino de Botânica na FURG por meio da organização e ampliação de coleções didáticas, utilizando recursos da web.
Login
Sumário
Ao longo dos anos, observa-se uma crescente ansiedade dos acadêmicos, no sentido de uma maior interação entre o material utilizado nas aulas práticas e o ambiente onde foram coletados. Faltando material que dê subsídios ao reconhecimento e a associação entre funções e constituição das estruturas presentes nas plantas e o ambiente de onde elas se originaram, a presente proposta mostra a preocupação com a formação acadêmica e com a preservação do meio ambiente.
Para a realização das aulas práticas de Botânica, são utilizados materiais frescos coletados principalmente no Campus Carreiros e região de entorno pelos técnicos do laboratório. Durante as aulas práticas, os materiais coletados são manuseados pelos acadêmicos, utilizados em experimentos de fisiologia vegetal ou em atividades que incluem a confecção de cortes histológicos a mão livre e montagem em lâminas para visualização ao microscópio das diferentes estruturas vegetais.
Outra atividade desenvolvida inclui a utilização de recursos didáticos disponíveis nos laboratórios de Botânica, como lâminas microscópicas semi-permanentes, exsicatas, carpoteca, sementário, coleções de algas, briófitas e fungos para comparação das estruturas a serem observadas. A disponibilização na web de coleções didáticas destinadas às aulas de Botânica para o Ensino de graduação elevará a qualidade do Ensino, como também irá minimizar as coletas de organismos para aulas práticas, além de facilitar ao acadêmico o acesso aos conteúdos tratados nas aulas práticas. Deste modo, contribuindo para o conhecimento e ao mesmo tempo com a preservação da flora característica dos diferentes ambientes que constituem o ecossistema costeiro do Sul do Rio Grande do Sul.
Visando facilitar a compreensão dos conteúdos abordados, a proposta foi dividida em dois capítulos: 1. Anatomia vegetal; 2. Fisiologia vegetal. Cada capítulo apresenta características específicas, sendo inicialmente subdivididos por ambientes e tecidos vegetais. Inicialmente foram trabalhadas plantas que ocupam o ecossistema das dunas.
A planície costeira do estado do Rio Grande do Sul destaca-se pelo seu extenso sistema de lagoas, banhados, matas ciliares e paludosas. Entre os ambientes costeiros, com influência do aporte de água salgada, destacam-se os marismas e as dunas. Nestes últimos, merece destaque a presença de uma elevada concentração de sais na água ou no solo, acarretando em um elevado potencial osmótico que dificulta a absorção de água pelas plantas. Além disso, as plantas que ocupam estes ambientes, ainda convivem com elevadas concentrações de sódio, carbonatos e íons clorídricos, as quais podem ser potencialmente tóxicas as plantas.
As dunas são feições naturais que se desenvolvem em praias arenosas. É característica destes ecossistemas a constante atuação de ventos oceânicos e o contínuo aporte de areia. Condições estressantes em função da movimentação do vento, da instabilidade da areia, da salinidade, da deficiência de nutrientes e do estresse hídrico, são fatores limitantes a ocupação destes ambientes pelas plantas. Assim, espécies que colonizam as dunas apresentam adaptações morfológicas, fisiológicas, reprodutivas e de ciclo de vida como resposta as condições estressantes impostas pelo ambiente.

Foto 1 - Blutaparon portulacoides - Habitat nas dunas da Praia do Cassino, Rio Grande, RS - Foto: Elton Colares
















